|
Коксохимическое производство. Слайд 20 из презентации «Основные источники углеводородов» к урокам химии на тему «Источники углеводородов». Коксохимическое производство. КОКСОХИМИЧЕСКОЕ ПРОИЗВОДСТВО. Важным источником промышленного получения ароматических углеводородов наряду с переработкой нефти является коксование каменного угля. Коксохимическое производство 24.11.15. Чтобы добавить отзыв, войдите в Ваш кабинет или зарегистрируйтесь. Скачать бесплатно презентацию на тему 'Коксохимическое производство. Что такое коксохимическое производство и для чего оно нужно? Основным его продуктом был и остается кокс, что следует из.' в формате.ppt (PowerPoint). Презентации по «Металлургии» на скачать презентацию бесплатно. Презентации охватывают все основные вопросы предмета «Химия». Изучение металлургии с помощью презентаций нацелено, прежде всего, на дальнейшую профориентацию учащихся, призвано помочь им выбрать будущую профессию. Школьников и студентов знакомят с целым рядом профессий металлургической промышленности, разъясняют, насколько значимое место занимают металлургические предприятия в народном хозяйстве. Не обойден стороной и вопрос экологического воспитания. Чтобы достичь наглядного изучения конкретных металлургических производств, экологических проблем и путей их решения воспользуйтесь возможностью скачать презентации по металлургии бесплатно на нашем сайте. Изучение химико- технологических основ получения металлов из руд, доменного производства, различных способов производства стали, производства легированных сталей, рационального использования сырья проходит значительно легче, когда подкреплено качественными презентациями на темы металлургии и металлургической промышленности. Аннотация к презентации. Презентация для школьников на тему 'Природный и попутный газ, их переработка. Коксохимическое производство' по химии. Презентация на тему: Природный и попутный газ, их переработка. Коксохимическое производство. Скачать эту презентацию. Нефть.Коксохимическое производство. Урок подготовлен с презентацией. Скачать Нефть.Коксохимическое производство. Бесплатное скачивание файла.  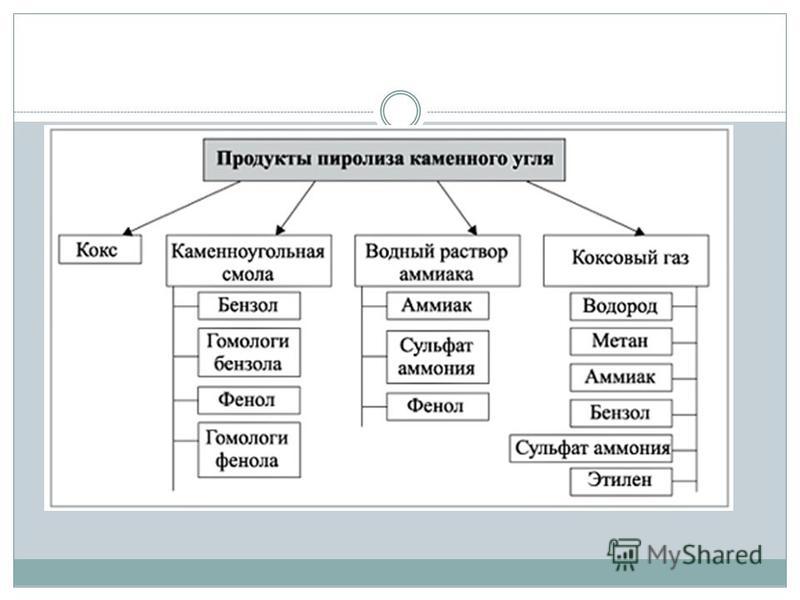
Исследуются перспективные технологии, применяемые для получения металлов, и производства чугуна и стали, а также виды рудного сырья, закономерности управления химическими реакциями, лежащими в основе металлургического производства, химизм и аппаратное оформление. Изучаются принципы металлургического производства, защита окружающей природы от загрязнения и охрана труда. В наших презентациях охвачены вопросы химического производства и экологии, современные направления развития химического и металлургического производства в России и за рубежом; вопросы малоотходных производств, коротких технологических циклов, утилизации отходов химической и металлургической промышленности, и прочее. Презентация по химии по теме: классификация уроков . Вводные. 2. Уроки изучения нового материала. Уроки формирования умений. Уроки контроля и коррекции. Комбинированные уроки. Уроки повторения изученного. Обобщающие уроки Слайд 3. Комбинированные уроки (смешанные) 1. Самые распространенные (7. Включают все основные элементы обучения в своей структуре; 3. Позволяют достигать нескольких целейурока и решать учебно – воспитательные задачи; 4. Недостатком этого урока является – дефицит времени (1. Слайд 4. Уроки изучения нового материала Используются для передачи объемов материала. Демонстрации технологических процессов, новых явлений; Формы уроков: лекции, объяснения, беседы, самостоятельные работы, постановка опытов; Структура урока ( организационное начало, постановка целей, изложение нового материала, выполнение практических работ, Д / З, Подведение итогов урока Слайд 5. Урок по изучению нового материала представлен в виде презентации по теме »Коксохимическое производство» Слайд 6. Работу подготовила: Ученица 1. Средней школы . Слайд 7. Основным сырьём для коксохимической промышленности служат угли. Структура и строение углей могут быть изучены при помощи микроскопа. Грубая структура угля, обнаруживаемая невооруженным глазом, называется макроструктурой. Обычный микроскоп позволяет видеть тонкую структуру угля, называемую микроструктурой. Кокс используется как источник тепла и как восстановитель в доменной плавке. При производстве кокса также образуются попутная продукция, в том числе сульфата аммония, смола каменноугольная, сырой бензол. Слайд 9. В углях можно различить более или менее однородную блестящую массу (витрен), сероватую массу (дюрен), содержащую различные включения, волокнистую часть (фюзен), похожую на древесный уголь, и минеральные включения. Витрен, дюрен и фюзен — основные компоненты угля, представляющие его петрографический состав. На коксохимические заводы уголь поступает обычно со многих шахт и углеобогатительных фабрик, и специалист должен не только знать свойства и состав углей, но и умело составлять из них смесь, которая дает наилучший кокс. Составление угольных шихт для коксования (шихтование) производится эмпирически. Одно из основных требований к качеству кокса — высокая прочность при достаточной крупности. Поэтому спекаемость угольной шихты как фактор, обеспечивающий высокую прочность коксового вещества, должна быть всегда достаточной. Коксохимическая промышленность отличается высокой концентрацией производства, т. Современные печи для коксования углей представляют собой горизонтальные прямоугольные камеры, выложенные из огнеупорного материала. Камеры течей обогреваются через боковые стены. Печи располагаются в ряд и объединяются в батареи для уменьшения потери тепла и достижения компактности. В типовую батарею печей с шириной камер 4. Обычные камеры имеют полезный объем 2. Ширина печей более 4. Для облегчения выталкивания кокса из камеры коксования ширину камеры со стороны выдачи кокса делают на 4. Таким образом, камера имеет вид конуса. Основные, конструктивные элементы коксовой батареи показаны на рис. За основные элементы батареи надо принять следующие: фундамент, регенераторы, корнюрную зону, зону обогревательных простенков, перекрытия простенков и перекрытия камер. Несмотря на быстрые темпы развития нефтехимической промышленности, коксохимия остается одним из основных поставщиков сырья для производства пластических масс, химических волокон, красителей и других синтетических материалов. Кроме того, на базе водорода коксового газа и азота кислородных станций металлургических комбинатов производятся самые дешевые азотистые удобрения. Водород является составной частью коксового газа, получаемого в значительном количестве при коксовании углей. Азот и кислород, составные части воздуха. Кислород нужен для интенсификации металлургических процессов. Азот кислородных станций может рационально использоваться в упомянутом комплексе, сочетающем черную металлургию и химическую промышленность. Химические продукты коксования используются также для производства химических средств защиты растений и животных. Более 2. 0 наименований продуктов и препаратов для нужд сельского хозяйства поставляет коксохимия. Ассортимент химических продуктов, выделяемых из каменноугольной смолы, сырого бензола и коксового газа насчитывает 1. Коксовый газ используется для обогрева коксовых печей и обеспечения других потребителей комбината. Средний расход сухой угольной шихты на 1 тонну сухого валового кокса составляет 1. Слайд 1. 4Изучение новой темы «Типы химических реакций» Слайд 1. Химические реакции Слайд 1. Учебная презентация Слайд 1. Типы химических реакций Слайд 1. По числу вступивших в реакцию веществ. По тепловому эффекту. По обратимости. По изменению степени окисления. По агрегатному состоянию веществ. По механизму Слайд 1. Na. OH + HCl = Na. Cl + H2. O Zn + 2. HCl = Zn. Cl. 2 + H2 2. H2. O = 2. H2 + O2 S + O2 = SO2 Два сложных вещества обмениваются своими составными частями Атомы простого вещества замещают атомы одного из элементов в составе сложного Из одного вещества получается несколько новых Из нескольких веществ получается одно новое Реакции обмена Реакции замещения Реакции разложения Реакции соединения Слайд 2. По числу вступивших в реакцию веществ Слайд 2. По тепловому эффекту Слайд 2. Экзотермические. Идут с выделение теплоты. S + O2 = SO2 + Q Слайд 2. Эндотермические. Идут с поглощением теплоты. N2 + O2 = 2. NO - Q Слайд 2. По обратимости Слайд 2. Необратимые. Идут только в одном направлении. Условия: образование осадка или слабого электролита (Н2. О), выделение газа, выделение большого количества теплоты Слайд 2. Обратимые. Идут одновременно в двух противоположных направлениях Слайд 2. По изменению степени окисления Слайд 2. Идут без изменения степени окисления элементов. Ca. CO3 = Ca. O + CO2 Слайд 2. Окислительно – восстановительные реакции. Идут с изменением степени окисления. Na + Cl. 2 = 2. Na. Cl Слайд 3. 0По механизму Слайд 3. Ионные. Na. OH + HCl = Na. Cl + H2. ONa+ + OH- + H+ +Cl- = Na+ + Cl- + H2. OH+ + OH- = H2. O Слайд 3. Свободнорадикальные. H2 + Cl. 2 = 2. HCl. Cl : Cl = 2. Cl. Cl. Слайд 3. 3По агрегатному состоянию веществ Слайд 3. Гомогенные. Между веществами нет поверхности раздела фаз. H2 + Cl. 2 = 2. HCl Слайд 3. Гетерогенные. Реакция идет на поверхности раздела фаз (т- г, т- ж, ж- г, т- т)С + О2 = СО2 Слайд 3. Урок формирования новых знаний и умений Задачи уроков направлены на: - развитие и формирование умений и навыков; - закрепление ранее усвоенных знаний; - коррекция знаний и умений. Достижение дидактических целей урока связано с организацией контрольно – оценочной функции. Слайд 3. 7Урок совершенствования новых знания Карточки с заданиями. Сообщения по теме. Практические работы. Самостоятельные работы. Презентации Видеоролики. Решение задач. Составление схем, диаграмм Слайд 3. Нестандартные уроки КВНВикторины. Деловые, ролевые и интеллектуальные игры. Общественные смотры знаний Слайд 3. Ролевая игра «Суд над алканами» Слайд 4. Видеоролики По химии (демонстрационные опыты)По ОБЖ (изучение нового материала).
0 Comments
Leave a Reply. |
AuthorWrite something about yourself. No need to be fancy, just an overview. Archives
July 2017
Categories |
 RSS Feed
RSS Feed
